معادلات التفاعلات الكيميائيّة - ملخّصات دروس العلوم الفيزيائيّة: السنة التاسعة أساسي
معادلات التفاعلات الكيميائيّة
ملخّصات دروس العلوم الفيزيائيّة
السنة التاسعة من التعليم أساسي
* أثناء كلّ تفاعل كيميائي تُحفظ المادّة. وهذا يعني أنّ مجموع كتلة التفاعلات أصبح مساويا لمجموع كتلة منتجات التفاعل.
مثال: تتفاعل 12g من الكربون مع 32g من الأكسجين لتنتج 44g من ثاني أكسيد الكربون.
* أثناء كلّ تفاعل كيميائي يحفظ العدد الجملي للذرّات من كلّ نوع.
مثال:
* تُكتب معادلة التفاعل الكيميائي باستعمال الرموز والصيغ الكيميائيّة للمتفاعلات ولمنتجات التفاعل.
مثال: احتراق الكربون في غاز الأكسجين يُنتج ثاني أكسيد الكربون.
ومعادلة التفاعل الكيميائي هي:
* توازن معادلة التفاعل الكيميائي بإضافة عدد صحيح طبيعي يُكتب قبل الصيغة الكيميائيّة لتتساوى عدد الذرّات من كلّ نوع بين المتقابلات ومنتجات التفاعل.
ملاحظات:
- الرقم 1 لا يُكتب في معادلة التفاعل الكيميائي.
- لموازنة معادلة تفاعل كيميائي يمكن ترك العنصر الموجود في جسم نقيّ بسيط للآخر.
مثال:
الأكسجين موجود في جسم نقي بسيط إذن توازن ذرّات الهيدروجين والكربون ونترك موازنة ذرّات الأكسجين للآخر فنحصل على:


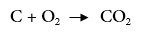


اتمنى ان توضح لنا الرموز بدقة اكثر وخاصة المعادلات طريقة فهمها صعبة
ردحذفMerci
ردحذفMerci
ردحذفأريد تعريف هذا التفاعل
ردحذف